V léčbě glaukomu se používají tyto skupiny léků: α-agonisté, β-blokátory, m-cholinomimetika, blokátory karboanhydrázy a analogy prostaglandinu. Než přejdeme k mechanismům jejich působení, je třeba vzít v úvahu některé rysy fyziologie oka.
Velikost zornice závisí na osvětlení a je regulována autonomním nervovým systémem.
Jasné světlo způsobuje miózu (konstrikci) a snížení osvětlení způsobuje mydriázu (rozšíření) zornice. Světlo vstupující do jednoho oka způsobuje zúžení zornice druhého oka. Tento reflex, nazývaný koordinovaná pupilární reakce, je výsledkem mozku. Ke koordinované pupilární reakci dochází pouze tehdy, když je mozek schopen zpracovat vizuální informace přijaté ze dvou sítnic, takže jde o užitečný diagnostický nástroj pro posouzení rozsahu poškození mozku u pacientů v komatu. Aktivita parasympatického nervového systému (PSNS) zužuje zornici. Stimulace sympatiku např. při strachu způsobuje mydriázu a snižuje vliv PSNS, i když v reflexní regulaci velikosti zornic stále převládá ten druhý. Radiální hladká svalovina duhovky, která rozšiřuje zornici, je inervována sympatickým nervovým systémem prostřednictvím vláken z horního krčního ganglia. Neurotransmiter norepinefrin a α agonisté1-adrenoreceptory radiálního svalu způsobují omezené rozšíření zornice (mydriáza). Kruhová hladká svalovina duhovky, která stahuje zornici, je inervována vlákny ciliárního ganglia PSNS. Neurotransmiterem je acetylcholin, který působí na muskarinové receptory. Léky, které stimulují M-cholinergní receptory, způsobují miózu a nazývají se miotika. Blokátory α-adrenergních receptorů (fentolamin aj.) se v klinické oftalmologické praxi používají jen zřídka kvůli omezené účasti norepinefrinu na regulaci velikosti zornice.
Kontrakce hladkého svalstva je důležitým prvkem fyziologické regulace oka.
Dilatace a zúžení zornice, tonus krevních cév a ciliárního svalu závisí na kontrakci hladkých svalů. Tyto procesy jsou regulovány různými částmi autonomního nervového systému pomocí různých mediátorů a receptorů. A α1, oni3-receptory aktivují Gq-proteiny, které naopak aktivují enzym fosfolipázu C ke kontrakci hladkých svalů.
Akomodace oka
Akomodace oka umožňuje upravit žáruvzdornou sílu a změnit dráhu světelného toku. Refrakční funkce tkání oka se obvykle měří v jednotkách optické refrakce – dioptrie. Největší refrakční systém oka se nachází na vnějším okraji rohovky a má pevnou hodnotu. Schopnost čočky měnit poloměr zakřivení zajišťuje zaostření obrazu na optickou část sítnice. Čočka v oční bulvě je podepřena ciliárním (ciliárním) svalem na závěsných (zinnových) vazech. Když se ciliární sval uvolní, tyto vazy vytáhnou čočku do elipsoidního tvaru. Malý poloměr zakřivení čočky umožňuje zaostření obrazu vzdálených předmětů na sítnici. Když se ciliární sval působením PSNS uvolní, čočka se stane sférickou. Zakřivení čočky se zvětšuje a blízké předměty se zaostřují na sítnici. Nepřetržité stahování ciliárních svalů zajišťuje přizpůsobení zrakové ostrosti, což vysvětluje únavu očí z dlouhého čtení. Během adaptace vidění se zorničky stahují a omezují tak vstup světelných paprsků do středu čočky. Dochází ke sférickému vychýlení a tím se zlepšuje kvalita obrazu na sítnici. K adaptaci zornic dochází reflexně. Prostředky blokující adaptaci oka (akomodační paralýza) se nazývají cykloplegici. Téměř všechny jsou M-anticholinergika. V souladu s tím M-mimetika způsobují kontrakci ciliárního svalu a spasmus akomodace. V ciliárním svalu nejsou žádné adrenoreceptory, proto ani sympatolytika ani sympatomimetika neovlivňují zakřivení zornice.
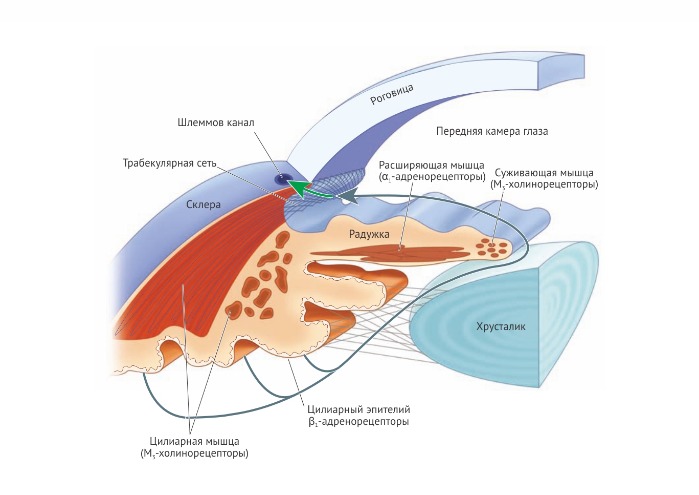
Zornice jsou schopny maximálního (asi 12 dioptrií) stupně adaptace v dospívání, pak tato schopnost postupně klesá, jak se čočka stává méně elastickou. Ve věku 50 let se akomodační schopnost čočky snižuje na 1 nebo 2 dioptrie, takže starší lidé obvykle potřebují brýle na čtení. Tento jev, nazývaný presbyopie (stařecká dalekozrakost), je přirozeným projevem stárnutí.
Proces tvorby nitrooční tekutiny
Přední komora oka je naplněna nitrooční tekutinou. Tvoří se v cévách řasnatého tělíska nepřetržitě v množství 3 ml/den. Tato tekutina vstupuje nejprve do zadní komory oka, poté přes zornici do přední komory. Většina z nich proudí do episklerálních žil přes trabekuly a Schlemmův kanál. Asi 10 % nitrooční tekutiny se vstřebá do tloušťky skléry. Tvorba a následný odtok nitrooční tekutiny udržuje nitrooční tlak v normálním rozmezí 12 až 20 mmHg. Umění. Tvorba nitrooční tekutiny nepřímo souvisí s krevním tlakem a prokrvením řasnatého tělíska. Aktivace α1-adrenergní receptory způsobují spasmus krevních cév v řasnatém tělísku a α2-receptory snižují tvorbu nitrooční tekutiny. Naopak aktivace β-adrenergních receptorů zvyšuje tvorbu nitrooční tekutiny.
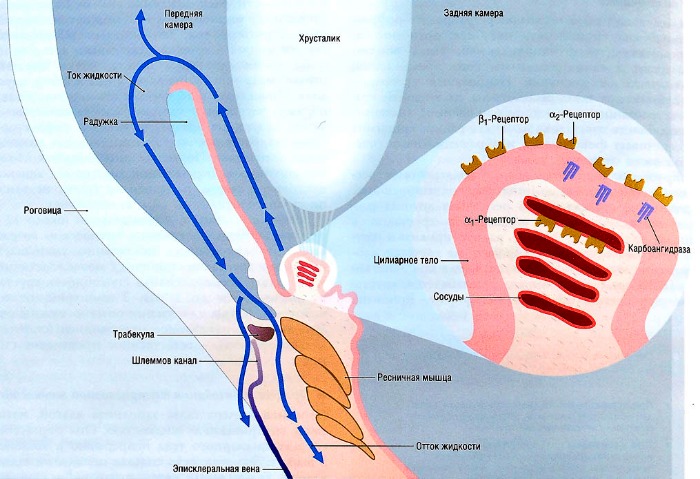
Karboanhydráza je enzym, který hraje důležitou roli při tvorbě nitrooční tekutiny.
Enzym karboanhydráza hraje důležitou roli při tvorbě nitrooční tekutiny. Jeho působení v orgánech zraku je podobné jeho působení v ledvinách nebo v jiných orgánech, kde se tvoří tkáňové tekutiny. Iontové složení nitrooční tekutiny je podobné jako v krevní plazmě, ale obsah bílkovin (10 mg/100 ml) je mnohem nižší než v plazmě (6000 mg/100 ml). Díky nízkému obsahu bílkovin je nitrooční tekutina průhledná. Nitrooční tekutina není ultrafiltrát plazmy, jak naznačuje vyšší obsah hydrogenuhličitanů a kyseliny askorbové v ní. Tento rozdíl ve složení naznačuje, že nitrooční tekutina je tvořena aktivnějšími procesy než filtrací. Tato skutečnost je důležitá pro pochopení toho, jak inhibitory karboanhydrázy snižují produkci komorové vody.
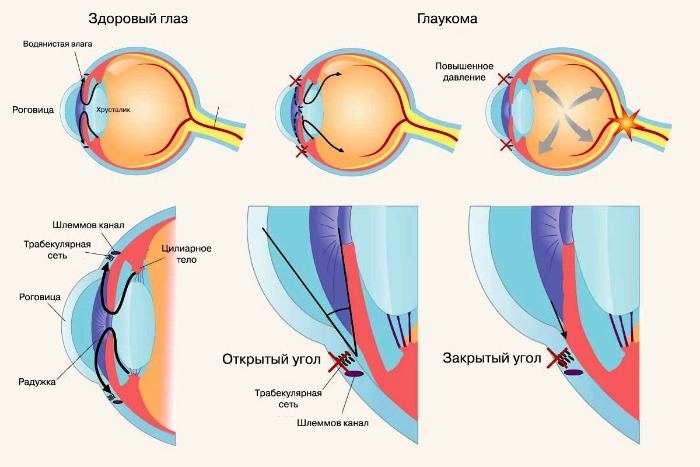
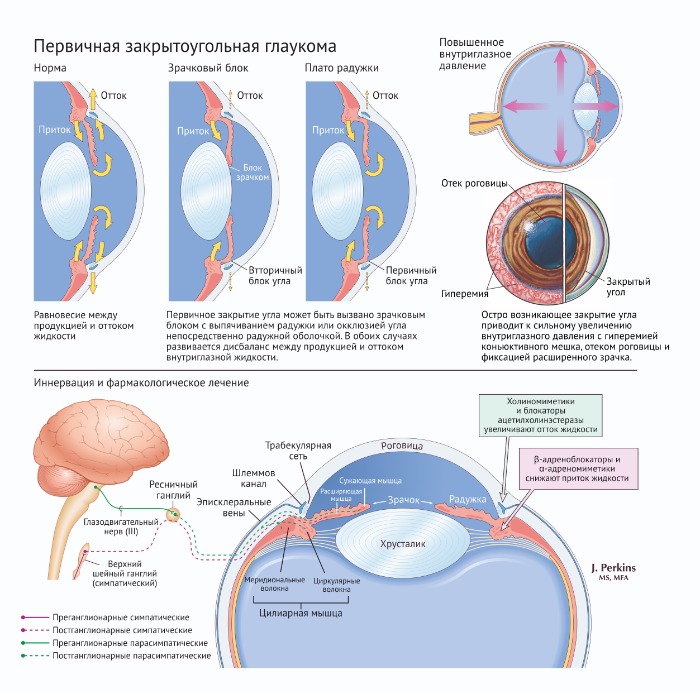
Příčiny glaukomu s uzavřeným úhlem, hlavní cíle léků a inervace oka
Farmakoterapie glaukomu
Glaukom je lékařský termín pro snížení funkce buněk sítnice, které končí progresivním snížením zrakové ostrosti a nakonec slepotou. Historicky byl tento stav spojován se zvýšeným nitroočním tlakem (IOP), ale poškození buněk sítnice může nastat bez zvýšení IOP. Tato léze se nazývá glaukom s normálním tlakem. Na druhou stranu zvýšení NOT nemusí poškodit sítnici. Snížení NOT je základem léčby glaukomu, ale konečným cílem terapie je zabránit ztrátě zraku.
Glaukom s otevřeným úhlem a glaukom s uzavřeným úhlem
Glaukom s otevřeným úhlem je chronické onemocnění způsobené poruchou odtoku nitrooční tekutiny do Schlemmova kanálu. V některých případech může být onemocnění vrozené. Farmakoterapie glaukomu je založena na dvou úkolech. Prvním je snížení tvorby nitrooční tekutiny, druhým zvýšení jejího odtoku. Glaukom s uzavřeným úhlem je spojen s některými anatomickými rysy duhovky, což vede k jejímu splynutí s čočkou, což je také doprovázeno porušením odtoku nitrooční tekutiny.
1. Prostředky, které snižují tvorbu nitrooční tekutiny
1.1. β-andrenoblokátory
β-blokátory jsou typickými léky volby používanými u glaukomu ke snížení tvorby nitrooční tekutiny. Propranolol se nepoužívá k léčbě glaukomu, protože má lokální anestetický účinek, zbavuje rohovku jejího ochranného reflexu. Neselektivní betablokátory používané při léčbě glaukomu (např.karteolol, levobunolol a timolol), stejně blok β1a β2 adrenoreceptory. Blokátory β-receptorů snižují tvorbu komorové vody blokováním β-receptorů v řasnatém tělísku a snižují účinek adrenalinu z dřeně nadledvin a norepinefrinu uvolněného z řasnatého tělíska. Ke snížení nitroočního tlaku se také používají selektivní β antagonisté.1-receptory, jako je betaxolol hydrochlorid. Betaxolol lze použít u pacientů s respirační patologií (astma atd.), ale farmakoterapie takových pacientů vyžaduje zvláštní sledování a opatrnost.
1.2. a-adrenergní agonisté
Tvorbu nitrooční tekutiny lze omezit i adrenomimetiky. Adrenalinový spěch není pro tento účel příliš efektivní, protože špatně se vstřebává z povrchu oka a rychle metabolizuje monoaminooxidázou. K tomu nedochází u proléčiva dipivefrin hydrochloridu. Je lipofilní a při vstupu do oka se působením rohovkových esteráz přemění na adrenalin. Mechanismus účinku epinefrinu (dipivefrinu) při snižování nitroočního tlaku nebyl přesně stanoven. Možná působí na β2-receptory v řasnatém tělese, způsobující pokles tvorby nitrooční tekutiny.
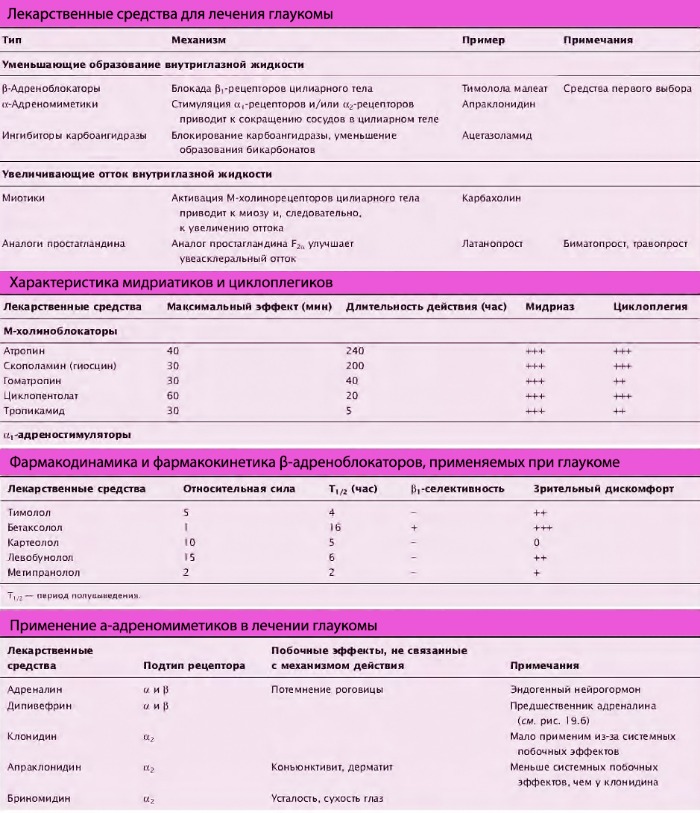
Adrenalin zpočátku zvyšuje nitrooční tlak, ale dlouhodobé užívání léku snižuje NOT; je pravděpodobné, že epinefrin znecitlivuje odpověď oka zprostředkovanou β-adrenergními receptory. Dlouhodobé užívání adrenalinu vede ke snížení prokrvení řasnatého tělíska aktivací α1-receptory v tepnách, což způsobuje vazokonstrikci a snížení rychlosti tvorby nitrooční tekutiny.
apraklonidin (derivát klonidinu) – selektivní α2-agonista, ale ve vysokých koncentracích aktivuje i α1-adrenoreceptory. Užívání apraklonidinu omezuje jeho nežádoucí účinky – zvýšený NOT, alergická konjunktivitida nebo dermatitida při dlouhodobém užívání (=40 % pacientů). Mechanismus účinku apraklonidinu, stejně jako adrenalinu, při snižování IOP je stále nejasný.
Existuje několik teorií:
- aktivace α2-adrenergní receptory v řasnatém tělese inhibuje aktivitu adenylátcyklázy, snižuje množství cAMP a tím snižuje tvorbu nitrooční tekutiny a zvyšuje uveosklerální odtok. Zvýšení uveosklerálního odtoku při dlouhodobém užívání lze vysvětlit zvýšeným uvolňováním prostaglandinu v důsledku α-adrenergní stimulace;
- aktivace α1-adrenergní receptory snižují průtok krve do řasnatého tělíska jako adrenalin;
- aktivace presynaptického α2-receptorů vede k omezení uvolňování adrenalinu a poklesu tvorby nitrooční tekutiny po poklesu excitace postsynaptických β-receptorů.
Zrudnutí, stažení očního víčka, konjunktivální vazokonstrikce a mydriáza jsou běžné nežádoucí vedlejší účinky léků s agonistou a-receptorů.
brimonidin – vysoce selektivní α2– adrenergní agonista. Snižuje nitrooční tlak snížením tvorby a zvýšením odtoku nitrooční tekutiny podél uveosklerální dráhy. Jeho účinnost je srovnatelná s timololem (účinek brimonidinu je o něco slabší). Nejčastějším nežádoucím účinkem je alergická konjunktivitida. V léku obsahujícím brimonidin “Alphagan R” používá se jako konzervant Puritová (jako alternativa k benzalkoniu), což zvyšuje snášenlivost léku.
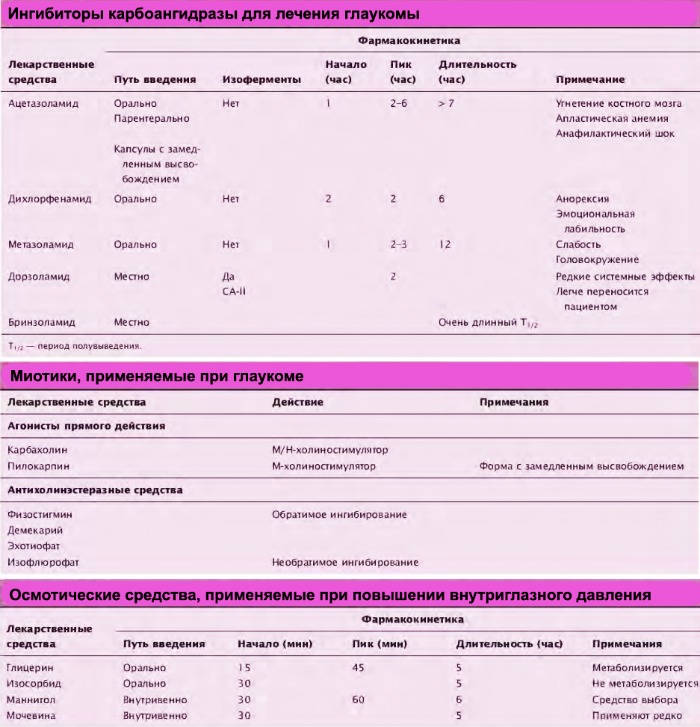
1.3. Inhibitory karboanhydrázy
Inhibitory karboanhydrázy jsou léky, které se užívají perorálně při léčbě glaukomu. Přeměnu oxidu uhličitého a vody na kyselinu uhličitou katalyzuje enzym karboanhydráza; rychlost konverze závisí na konkrétní izoformě enzymu. Protože tvorba nitrooční lékové tekutiny závisí na aktivním transportu bikarbonátu a Na iontů, omezení aktivity karboanhydrázy snižuje tvorbu nitrooční tekutiny.
Derivát sulfonamidu acetazolamid, syntetizovaný již v 1950. letech XNUMX. století, je inhibitor karboanhydrázy, který účinně snižuje IOP. Kvůli nežádoucím účinkům je však jeho použití omezené. Nežádoucí účinky, zejména u starších osob, mohou zahrnovat parestezie, hypokalemii, sníženou chuť k jídlu, ospalost a depresi. Závažnost těchto účinků je mnohem menší u nových léků s pomalým uvolňováním léku. Snížení frekvence nežádoucích účinků může být způsobeno nižšími maximálními koncentracemi léčiva.
Inhibitor karboanhydrázy dorzolamid blokuje specifickou izoformu karboanhydrázy – karboanhydrázu II, izolovanou v řasnatém tělísku a erytrocytech. Dorzolamid se doporučuje kombinovat s β-blokátory a miotiky.
2. Léky zvyšující odtok nitrooční tekutiny
2.1. miotika
Miotika zlepšují odtok nitrooční tekutiny v důsledku zvýšené uveasklerální drenáže, ale mají nepříznivý vliv na zúžení zornic, což může zhoršit vidění ve tmě. Chronická akomodační křeč způsobená miotiky může časem vést k rozmazanému vidění a bolestem hlavy. Tyto nežádoucí účinky se vyskytují u většiny pacientů, ale u starších pacientů obvykle časem ustupují. Lékové formy s prodlouženým uvolňováním účinné látky (například prodloužená forma M-cholinomimetika pilokarpin) mají minimální vedlejší účinky u mladších pacientů. Na rozdíl od očních kapek nevytvářejí lékové formy s prodlouženým uvolňováním vysokou počáteční koncentraci léčivých látek.
2.2. Analogy prostaglandinu
latanoprost – syntetický analog prostaglandinů, který zvyšuje uveasklerální odtok stejným mechanismem jako endogenní prostaglandin PG2a. Jeho působení je spojeno s relaxací ciliárního svalu. Úspěch latanoprostu vedl k vytvoření jeho protějšků, bimatoprostu a travoprostu. Nežádoucí účinky: překrvení spojivek, zvýšený růst řas, pigmentace duhovky a podráždění očí.
tafluprost – fluorovaný analog prostaglandinu F2α. Je hydrolyzován karboxylesterázou za vzniku aktivního metabolitu kyseliny tafluprostové, který má vysokou aktivitu a selektivitu pro prostaglandinové F-receptory (afinita k receptorům je 12krát vyšší než u lanaprostu).
Mezi další léky v této skupině patří bimatoprost (syntetický prostamid strukturně podobný PGF2α, který napodobuje účinky prostamidů) a travoprost (syntetický analog PGF2α).
Účinnost léků v léčbě glaukomu.
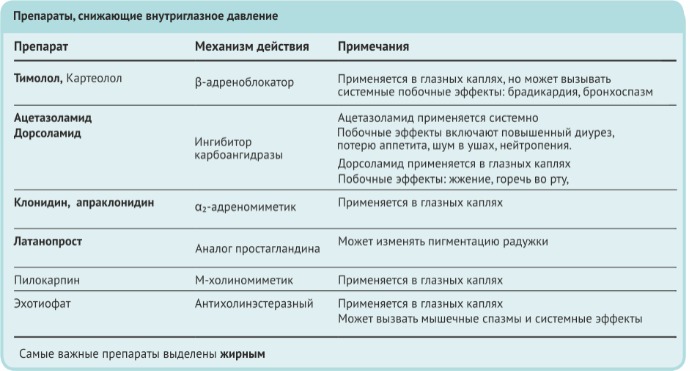
Ve srovnávacích testech byly inhibitory karboanhydrázy stejně účinné jako sympatomimetika. Klinická účinnost však není jediným faktorem určujícím výběr léku, je třeba vzít v úvahu i nežádoucí účinky a individuální charakteristiky pacienta. Léky první volby jsou analogy prostaglandinu (latanoprost, travoprost) a timolol. Do druhé linie farmakoterapie patří inhibitory KA, α-agonisté a β-blokátory.
3. Vlastnosti terapie
3.1. Farmakoterapie glaukomu s otevřeným úhlem.
Taktika léčby glaukomu je založena na stanovení rizikových faktorů a faktu progrese glaukomové neuropatie zrakového nervu a jejich ovlivnění. Vzhledem k tomu, že hlavním faktorem v patogenezi a smrti gangliových buněk sítnice u glaukomové neuropatie zrakového nervu je zvýšení nitroočního tlaku nad individuálně tolerovanou úroveň, je hlavním úkolem v léčbě glaukomu snížit IOP na cílovou úroveň. Cílový tlak je horní úroveň tonometrického NOT, při které je možné zastavit nebo zpomalit poškození vnitřních struktur oční bulvy a rozpad zrakových funkcí. Cílový tlak by neměl překročit tolerantní IOP (horní hranici normálního IOP vlastní tomuto pacientovi, nad kterou se stává patologickým). Cílový tlak je stanoven s přihlédnutím ke všem rizikovým faktorům každého jednotlivého pacienta jako výsledek podrobného vyšetření a sledování dynamiky zorného pole a změn v terče zrakového nervu. Pro 75 % zdravých jedinců je normální IOP 20-21 mmHg.
Optimální lék pro léčbu dosud nebyl nalezen. Obvykle se terapie zahajuje β-blokátory, pokud však není dosaženo cílového NOT, přidávají se k terapii miotika a sympatomimetika. Zdá se paradoxní používat jak β-blokátory, tak agonisty stejných receptorů u stejného pacienta, ale jak bylo popsáno dříve, tyto látky pravděpodobně působí prostřednictvím různých mechanismů snižujících nitrooční tlak a mohou mít kombinované účinky. Inhibitory karboanhydrázy se obecně používají jako léky třetí linie, protože mohou mít významné nepříznivé účinky. Inhibitory karboanhydrázy, jako je dorzolamid, se mohou více používat. Latanoprost umožňuje farmakoterapii přetrvávajících případů zvýšeného NOT. Bimatoprost, agonista PG2α receptoru, se používá lokálně v léčbě glaukomu (0,03% roztok), stejně jako travoprost. V konečném důsledku závisí výběr léku na glaukom na charakteristice průběhu onemocnění u konkrétního pacienta. Například antagonisté β-receptorů jsou kontraindikováni u pacientů s astmatem. V mladém věku a u pacientů se zvýšeným rizikem odchlípení sítnice je třeba myotika používat s opatrností.
3.2. Farmakoterapie glaukomu s uzavřeným úhlem
V kritické situaci se používají léky, které nepřímo snižují nitrooční tlak. IV mannitol (osmotické diuretikum) a perorální glycerin zvyšují osmolaritu krve a mohou rychle snížit vysoký nitrooční tlak, který bezprostředně ohrožuje zrak. Miotika, jako je pilokarpin nebo karbacholin, mohou výrazně protáhnout duhovku a dočasně snížit IOP. Hyperosmotika snižují IOP snížením objemu sklivce. Zvýšení osmolarity plazmy způsobí odtok vody ze sklivce do nitroočních krevních cév, čímž se jeho velikost zmenší o 10 %. To umožňuje snížit IOP a prohloubit přední komoru oka díky pohybu duhovky, což je zvláště užitečné.
Zdroje:
- Clive Page „Farmakologie. Klinický přístup“ 2012
- Robert B. Raffa, Netter’s Illustrated Pharmacology Updated Edition 2013
- Robert B. Raffa, Rang & Dale’s Pharmacology, 8e 2015
- Kanskiho klinická oftalmologie, 8. vydání Systematický přístup 2016
- Medscape














